Un fallo frecuente en química orgánica cuando nos iniciamos es no distinguir el benceno y el ciclohexano. Las moléculas se parecen porque ambas son moléculas con 6 carbonos, pero es lo único en lo que se parecen.
Para empezar la fórmula empírica del ciclohexano es C6H12 mientras que la fórmula empírica
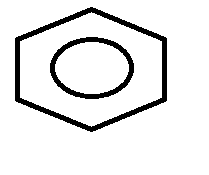
del benceno es C6H6. El ciclohexano es un cicloalcano, mientras que el benceno es un anillo aromático. El benceno es un ciclo que tiene tres dobles enlaces que se están moviendo continuamente en el espacio, por eso se representa con un O en el medio.
Las moléculas son también estructuralmente distintas. Un ciclohexano podemos girar sus enlaces obteniendo distintas conformaciones.
 |
| Ciclohexano |
El ciclohexano tal y como lo vemos en la imagen, se puede "doblar" y obtenemos una conformación denominada conformación silla.
 |
| Ciclohexano en conformación silla |
 |
| Ciclohexano en conformación silla |
Si intercambiamos las posiciones en las que están los hidrógenos respecto a unos y otros obtenemos otra conformación silla.
 |
| Ciclohexano en conformación bote |
También se puede doblar de modo que quede otra conformación, que es denominada conformación bote.
 |
| Ciclohexano en conformación bote |
Es necesario pasar por la conformación bote, para interconvertir una conformación silla en otra.
El ciclohexano en el espacio se dibujaría:
El benceno al contrario del ciclohexano es una molécula completamente plana.

Los enlaces cuesta mucho trabajo girarlos sin romperlos, por lo que el benceno no tiene conformaciones posibles.
Un benceno representado en el espacio sería:
 |
| Benceno en el espacio |
Pero a la hora de formular, tendemos a representar el benceno en el plano que sería:
 |
| Benceno en el plano |
En la foto del artículo se representa el benceno como:
Esta notación es correcta, aunque está tendiendo a desaparecer. Indica que los enlaces se están moviendo en el espacio y hay varias formas resonantes posibles.
Posiblemente esa representación con el círculo dentro, al acostumbrarse a hacerla, nos hace olvidarnos su significado, los dobles enlaces y esto es lo que hace que haya confusiones cuando uno se inicia en el estudio de la química orgánica.
Descubrirlaquimica. Estudiante de química en la USC
17/01/2015
Este artículo participa en la XLIII edición del carnaval de la química alojado en el blog La ciencia de la vida